Date: December 2020
利用免疫系统固有的抗肿瘤活性对抗癌症的疗法的出现代表着肿瘤疗法的一种范式转变,这种转变永久改变了我们未来对抗癌症的方式。
结直肠癌(CRC)在整个癌症疾病中比例可观,占所有癌症病例的10%;2018年,全球新增CRC病例超过100万,导致逾50万人死亡1。对于非转移性结肠癌,临床治疗包括外科手术切除和辅助化疗,以及针对转移性CRC2的靶向治疗。近期的临床研究表明,在无法切除、具有高度微卫星不稳定性(MSI-H)的转移性,或错配修复缺陷(dMMR)的大肠癌患者中,免疫检查点抑制可发挥强大效果3。由于临床功效强大,2020年夏季,针对人PD-1免疫检查点蛋白的单克隆抗体Keytruda已通过批准,用作满足这三个标准的CRC患者的一线治疗4。由于针对CRC的免疫疗法带来了新的希望,就需要采用针对该疾病的高度转化性临床前模型来评估新型免疫肿瘤学药物的有效性。
评估针对免疫系统的疗法的功效需要临床前肿瘤模型,这种模型要具有完好的免疫系统,以便使用受试试剂进行操控。同基因肿瘤模型代表着这样一种策略,即,使小鼠衍生的癌细胞生长,以在肿瘤细胞来源、具有免疫活性的小鼠品系中形成肿瘤。 We have extensively used CT26.WT murine colon carcinoma as a subcutaneous tumor model in female Balb/c mice to evaluate the efficacy of immuno-oncology agents - see our previous work in the model spotlights below (additional data available upon request):
我们认识到皮下肿瘤模型的实验和转化局限性——与原位器官产生的肿瘤相比,它具有不同的肿瘤微环境,包括但不限于会影响免疫治疗反应的不同免疫细胞概况5,6。将肿瘤细胞植入原位组织中(称为原位肿瘤植入物)旨在消除皮下研究的局限性并增加模型的潜在可转化性。
在此模型中,我们将提供能证明可靠且可复制的原位鼠肿瘤模型的数据,这种模型采用CT26.WT结肠癌、可靠的植入手术方法并且能够验证对检查点抑制的反应。
所有动物研究均已获得实验动物关怀与使用委员会的批准,并按照AAALAC认可的计划中的实验动物关怀与使用指南进行,所有研究均有预先确定的人道安乐死标准。
CT26.WT-luc肿瘤的原位生长
图1. 原位植入Balb/c小鼠的CT26.WT-luc衍生肿瘤的生长动力学
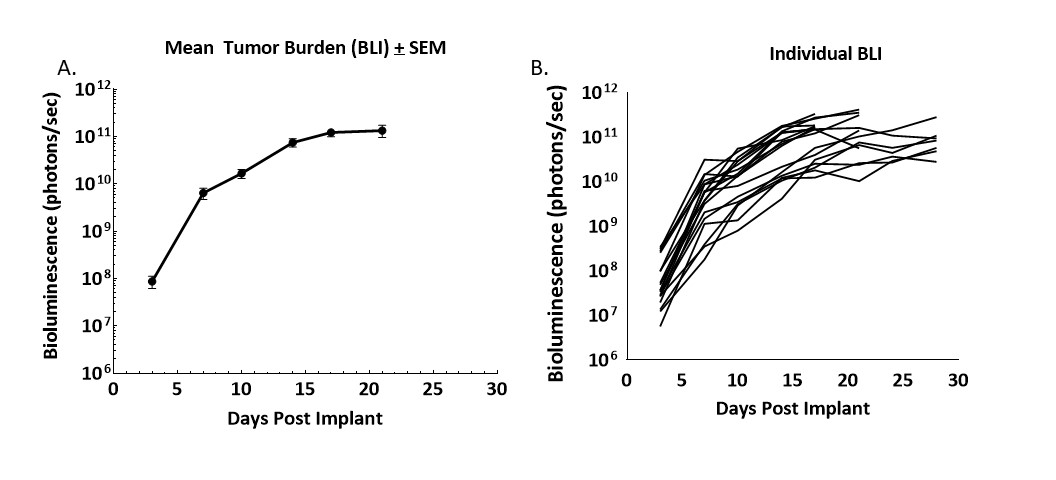
图1 - 通过20 Balb/c小鼠的生物发光成像对原位植入CT26.WT-luc肿瘤片段后的肿瘤负荷进行纵向监测。植入后三天开始检测生物性发光,展示了小组平均值(A)和个体值(B)。
肿瘤负荷进展稳健并且变化很小。基于BLI和尸检,肿瘤植入率为95%,未观察到自发消退。BLI衍生肿瘤体积倍增时间(Td)为1.5天,研究的中位时间为21天。
与疾病进展相关的常见临床观察结果是由于肿瘤生长和体重增加引起的腹胀(数据未显示)。尸检显示盲肠上有大量原发肿块,肝和腹壁上有小结节。观察到结肠上的原发性肿瘤与结肠具有大规模血管整合,表明肿瘤进行了有效的血管募集。我们的下一个方法是利用此模型确定免疫肿瘤学药物的功效。
原位CT26.WT-luc肿瘤模型的检查点抑制
如前所述,对原始态Balb/c小鼠进行了CT26.WT-luc肿瘤片段的手术植入。手术后三天通过BLI对动物进行分期,并根据BLI值将其分配到治疗组中。 Animals were treated by intraperitoneal administration of 10mg/kg isotype control (clone LTF-2), anti-mPD-L1 (clone 10F.9G2), anti-mCTLA-4 (clone 9D9) or anti-mPD-1 (clone RMP1-14) twice weekly for two weeks.所有抗体均购自BioXCell(美国新罕布什尔州莱巴嫩)。动物监测方法包括每周两次的BLI肿瘤负荷测量、每周三次的体重测量、每日临床观察以及最终尸检观察。
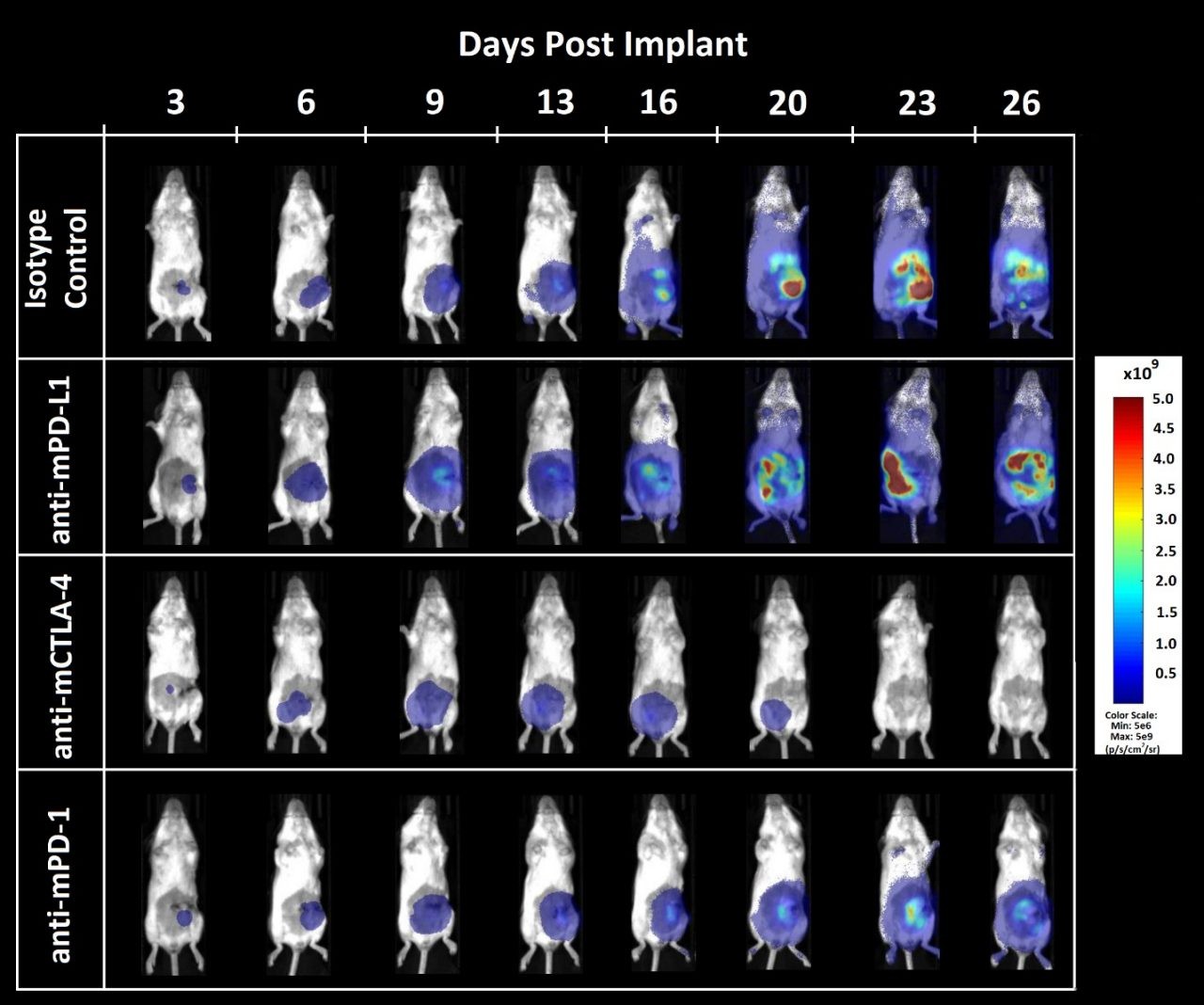
图2 - 原位植入的CT26.WT-luc肿瘤对检查点阻断抗体的反应。在对指定疗法的反应中,通过BLI(A)和动物个体BLI值(B-E)评估的小组平均肿瘤负荷。
给予同型对照抗体对肿瘤负荷或疾病进展没有影响(图2A,2B)。接受同种型对照抗体的动物的肿瘤倍增时间为2.2天,研究的中位时间为28天。给予抗mPD-L1(图2A,2C)导致一次完全消退(在背景BLI值以上没有可检测到的肿瘤负荷)。抗mCTLA-4治疗(图2A,2D)导致第23日ΔT/ΔC为0.1%和五次局部消退(BLI值小于治疗第一天的一半),尸检时没有明显可见的疾病。给予抗mPD-1(图2A,2E)不会导致肿瘤消退或无肿瘤幸存者。
图3. CT26.WT-luc原位肿瘤对检查点抑制的反应的生物发光成像
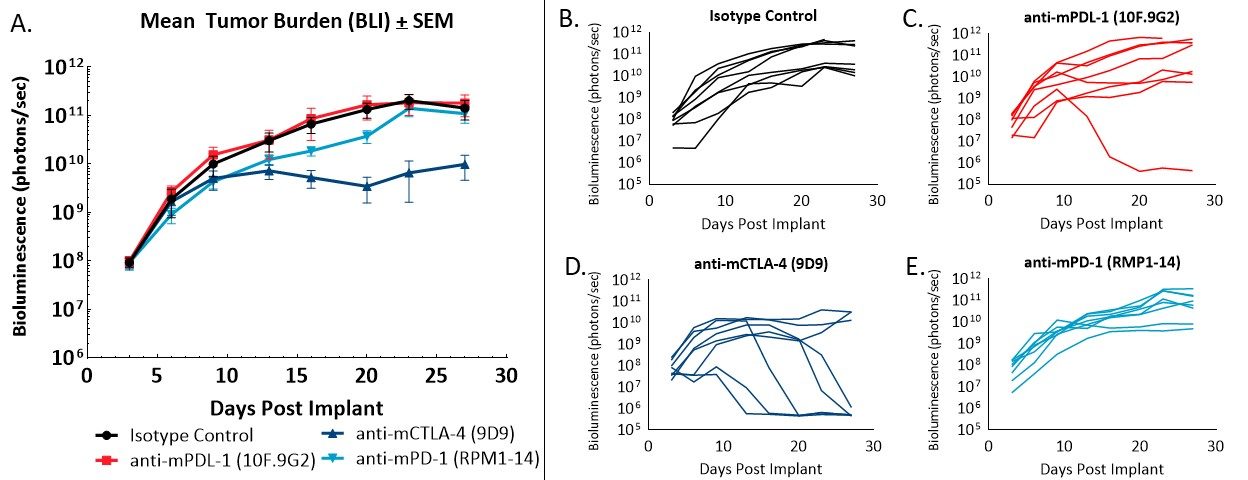
图3 - 原位植入雌性Balb/c小鼠的CT26.WT-luc衍生肿瘤经免疫检查点阻断治疗的生物发光成像。展示的动物代表每个相应组的中位BLI值。
根据先前的先导性生长实验(数据未显示),肿瘤负荷局限于腹部并随时间推移增加(图3)。抗mCTLA-4治疗导致疾病相关体重增加的发作延迟(数据未显示)。相比同种型对照抗体,使用抗mPD-L1或抗mCTLA-4治疗的寿命更长,分别为12.5和23.6天。终末尸检显示,在接受抗mPD-L1和抗mCTLA-4治疗的动物中,分别有1/8和5/8没有肿瘤或其他病变的迹象。
正在进行的工作是评估皮下和原位CT26.WT植入位置之间在肿瘤免疫细胞浸润、组织学特征和形态以及响应检查点阻断的免疫活性方面的差异。
综上所述,我们已经证明了CT26.WT-luc结肠癌原位模型为评估高度转化性植入位置的免疫肿瘤药物提供了一个强大的平台。
Contact our scientists to learn more about the CT26.WT-luc, and other murine orthotopic tumor models, and how we can apply these tools to advance your oncology pipeline.
参考资料
1Bray F等人。2018年全球癌症统计:GLOBOCAN估测36种癌症在全球185个国家的发病率和死亡率。CA Cancer J Clin 2018; 68:6, 394-424。
2Kuipers E等人。结直肠癌。Nat Rev Dis Primers. 2015; 1: 15065。
3Tintelnot J, Stein A. 结直肠癌免疫治疗:可用的临床证据、挑战和新方案。World J Gastroenterol. 2019; 25:29, 3920-3928。
4食品及药物管理局。FDA批准了MSI-H/dMMR转移性结直肠癌患者的一线免疫治疗。新闻稿,2020年6月29日。
5Devaud C等人。不同解剖部位的组织可以塑造和改变肿瘤的微环境,从而影响对治疗的反应。Mol Ther. 2014; 22:1, 18-27。
6Zhao X、Li L、Starr TK、Subramanian S。肿瘤部位影响结肠癌小鼠模型的免疫反应。Oncotarget 2017; 8:33, 54775-54787。
7Fiegle E、Doleschel D等人。CTLA-4和PDL-1双重阻断在结肠癌的高度侵袭性原位小鼠模型中抑制肿瘤生长和肝转移。 Neoplasia 2019; 21:9, 932-944
让我们开始对话
联系我们