Author: Mark J Cameron, Director of Scientific Development
Date: November 2020
在临床前研发过程中,经常使用小鼠作为测试对象来研究CAR(嵌合抗原受体)T细胞疗法。在这种情况下,免疫功能低下的小鼠携带着人源性肿瘤负荷,并接受同种异体人类CAR T细胞给药。在工程化嵌合抗原受体的引导下,过继转移细胞与肿瘤细胞的表面抗原(例如CD19)结合。
由于工程化T细胞与肿瘤细胞结合,T细胞在MHC不受限制的区域中活化并杀死肿瘤细胞。 Mice in preclinical research studies are followed for a number of predefined parameters, evaluating tumor growth and burden to determine the efficacy of the CAR T cells (Learn more about how efficacy can be determined by bioluminescence imaging (BLI).
CAR T细胞抗肿瘤反应成功的关键因素是向宿主输注后CAR T细胞存在的时间长度(持续存在性)。 Despite full functionality, it has been shown that poor persistence of CAR T cells can limit an effective antitumor response.1 In the clinical setting, long-term remission in patients with hematological malignancies is associated with sustained persistence of CAR T cells.2 Co-stimulatory signaling is thought to influence T cell expansion and persistence. Preclinical studies investigating the efficacy of CAR constructs that are engineered to include the 4-1BB co-stimulator domain have been associated with long CAR T cell persistence, a slower and sustained effector function, and a higher proportion of memory T cells.3 Assessing CAR T persistence in preclinical studies have implications in determining clinical success.
本技术聚焦将为读者提供有关在临床前环境中使用流式细胞术测量CAR T细胞持续存在性的信息。
针对CAR T细胞候选评估的小鼠模型
2017年9月,美国食品药品监督管理局批准了首个CAR T细胞疗法。此细胞疗法由诺华公司销售,名为Kymriah。Kymriah也被称为tisagenlecleucel ,已被批准用于不再对B细胞急性淋巴细胞白血病的标准疗法产生应答的儿童和年轻人。Kymriah基于宾夕法尼亚大学的Carl June博士针对NSGTM小鼠开展的研究工作。
NOD.Cg-Prkdcscid Il2rgtm1Wjl/SzJ小鼠,俗称NOD scid gamma (NSG™),不表达Prkdc基因,也不表达X连锁的Il2rg基因。scid(严重联合免疫缺陷)突变位于DNA修复复合蛋白Prkdc中,导致小鼠B细胞和T细胞缺乏。这些小鼠没有补体细胞或自然杀伤(NK)细胞,并且细胞因子信号传导通路不足。这些缺陷使这些小鼠成为理想的选择,并且高度适合植入人体免疫细胞(包括CAR T细胞)。小鼠植入了多种人类肿瘤,并且是临床前CAR T细胞研究的黄金标准。
在我们的临床前肿瘤学部门,我们可以使用任何市售的小鼠品系进行CAR T细胞疗法和其他过继性细胞移植研究,包括NSGTM小鼠,在某些条件下,我们也可以接受特种小鼠。
来自临床前肿瘤学的PersistenceTTM 试剂盒最少只需5 uL全血便可生成纵向CAR T细胞持续存在性数据。它采用具有绝对计数的裂解/免清洗的测定法形式。该试剂盒具有灵活性,可以在FITC、PE和APC通道中添加特定的抗CAR探针。杰克逊实验室(美国缅因州巴港)的NSG小鼠被给予了2x107人类PBMC,在给药后7、14和21天抽取全血,并接受PersistenceTTM试剂盒评估。
表1介绍了PersistenceTTM试剂盒中使用的试剂。图1详细介绍了门控策略。
抗体/染料 |
描述 |
|---|---|
mCD45 |
小鼠全造血细胞 |
hCD45 |
人类全造血细胞 |
hCD3 |
人类pan-T细胞标记物 |
hCD4 |
人类CD4+ T细胞标记物 |
hCD8 |
人类CD8+ T细胞标记物 |
计数微珠 |
提供绝对计数 |
活性染料 |
死细胞排除 |
可选:CAR特异性 |
FITC、PE或APC |
表1:PersistenceTTM抗体试剂盒及其使用说明。
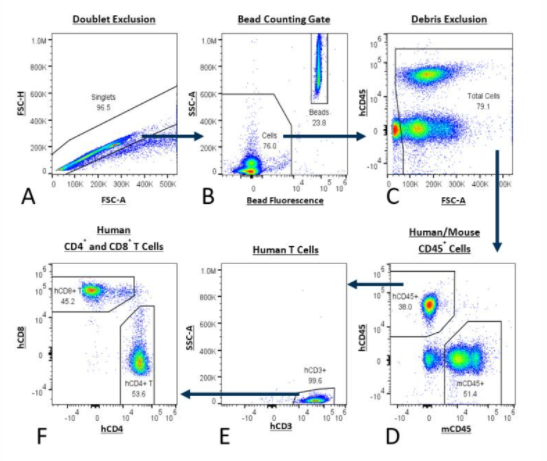
图1:使用PersistenceTTM试剂盒分析人类T细胞。门控策略从双重排斥(A)开始,然后转向结合微珠荧光和微珠计数门(B)。排除下一个细胞碎片(C),并使用具有抗人CD45(D)的抗小鼠CD45将小鼠细胞与人类细胞区分开。通过抗人CD3门控(E)分离人T细胞,最后确定人CD8+和CD4+ T细胞的数量(F)。
使用PersistenceTTM试剂盒对CAR T细胞进行纵向免疫表型鉴定
在临床肿瘤学环境中,CAR T细胞的扩增和持续存在性与患者的应答和获得缓解有关。4 由于这一发现,建立可靠的CAR T细胞数量跟踪方法尤为重要,不仅在评估CAR T细胞疗法的有效性方面,而且在临床前环境中的安全性评估方面也是如此。 Serious side effects of clinical CAR T cell therapy are noted, one of the most severe being cytokine release syndrome (CRS) and is associated with CAR T cell expansion in vivo.5
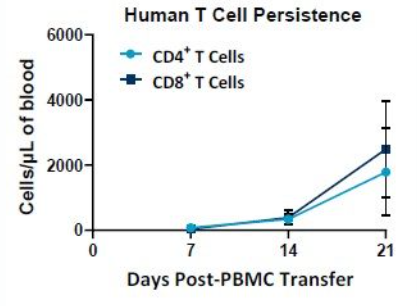
The PersistenceTTM Panel is directly applicable to the evaluation of human CAR T cell numbers in samples taken from mice over time.由于全血需求量低,因此可以多次从同一只小鼠中采集样本,也可以使用一组小鼠来达成研究目标。NSG小鼠可能会接受长期研究,以进行有针对性的CAR T持续存在性评估。图2显示了如何使用PersistenceTTM试剂盒测量随时间推移NSG小鼠中人类T细胞的实例。
改善CAR T细胞的持续存在性
体内CAR T细胞的持续存在性是CAR T细胞疗法长期临床疗效的替代指标。研究表明,某些含有CD28共刺激域的CAR T细胞表现出与T细胞衰竭相关基因的表达增加,而具有相同抗原特异性的4-1BB(TNFSF9)共刺激域减少了耗竭表型。这可能有助于解释为什么在针对患有复发性或难治性急性淋巴细胞白血病的患者的临床试验中,表达CD28域的CAR T细胞据报告可持续存在长达3个月,而具有4-1BB域的CAR T细胞可持续存在长达5年,几乎可以评估的所有案例都超过6个月。6
多代CAR T细胞
CAR T细胞通过嵌合抗原受体的修饰而继续进化。每个CAR T细胞都有一个scFv(单链片段变量)。scFv是重链(VH)可变区和轻链(VL)可变区的组合。scFv是免疫球蛋白的VH和VL的融合蛋白,与10和25氨基酸之间的短接头肽连接。
第一代CAR具有细胞外结合域、铰链区、跨膜域和一个或多个细胞内信号传导域。所有CAR T细胞都具有用于细胞内信号传导的CD3 ζ链域,并且是T细胞激活信号的主要发送者。共刺激域(CD28或4-1BB)是第二代CAR的特征。目的是改善T细胞增殖、细胞因子分泌和体内持续存在性。
临床前数据表明,与第二代CAR相比,第三代CAR具有更好的效应子功能和更长的体内持续存在性。第三代CAR具有多个共刺激域(CD28-41BB或CD28-OX40)。装甲CAR和TRUCK(杀死普遍细胞因子的重定向CAR T细胞(CAR T cells redirected for universal cytokine killing))是有时用于第四代CAR T细胞的名称。第四代CAR T细胞可以包含增强T细胞扩增、抗肿瘤活性和持续存在性的因子。7
无论哪一代CAR或TRUCK,PersistenceTTM试剂盒均是在临床前环境中短期或长期监测体内CAR T细胞持续存在性的出色工具。
总结
使用科文斯临床前肿瘤学的PersistenceTTM试剂盒可轻松测量CAR T的持续存在性。我们的流式细胞术试剂盒可从少量血液中确定纵向CAR T的持续存在性。我们的人类CompTTM试剂盒(表2)是一个很好的例子,说明了如何将其他符合资格要求的试剂盒添加到临床前CAR T研究中,以生成全面的流式细胞术数据集。
抗体/染料 |
描述 |
|---|---|
hCD45 |
人类全造血细胞 |
hCD3 |
人类pan-T细胞标记物 |
hCD4 |
人类CD4+ T细胞标记物 |
hCD8 |
人类CD8+ T细胞标记物 |
hCD25 |
人类调节性T细胞标记物 |
hFoxP3 |
人类调节性T细胞标记物 |
hPD-1 |
人类T细胞抑制信号传导蛋白 |
hCD69 |
活化标记物 |
Ki-67 |
增殖标记物 |
活性染料 |
死细胞排除 |
表2. 人类CompTTM白细胞试剂盒中的单个标记物。
To learn more about how the PersistenceTTM Panel, or one of our other flow cytometry panels, can be incorporated into your preclinical oncology research and to learn more about our extensive flow cytometry program contact the scientists.
参考资料
1Song DG, Ye Q, Carpenito C, Poussin M, Wang LP, Ji C, Figini M, June CH, Coukos G, Powell DJ Jr. In vivo persistence, tumor localization, and antitumor activity of CAR-engineered T cells is enhanced by costimulatory signaling through CD137 (4-1BB).
Cancer Res. 2011年7月 1;71(13):4617-27。
2Maude SL、Frey N、Shaw PA、Aplenc R、Barrett DM、Bunin NJ等人。嵌合抗原受体T细胞可实现白血病持续缓解。N Engl J Med. 2014;371(16):1507-17。
3Long AH、Haso WM、Shern JF、Wanhainen KM、Murgai M、Ingaramo M等人。4-1BB共刺激可改善嵌合抗原受体的强直信号诱导的T细胞衰竭。Nat Med. 2015;21:581-90。
4Porter DL、Hwang WT、Frey NV、Lacey SF、Shaw PA、Loren AW等人。嵌合抗原受体T细胞在复发性难治性慢性淋巴细胞性白血病中持续存在并诱导持续缓解。Sci Transl Med. 2015;7(303):303ra139。
5Santomasso B、Bachier C、Westin J、Rezvani K、Shpall EJ。CAR T细胞疗法的另一面:细胞因子释放综合征、神经毒性和经济负担。
Am Soc Clin Oncol Educ Book. 2019年1月;39:433-444。
6Maus MV and June CH. Making Better Chimeric Antigen Receptors for Adoptive T-cell Therapy.Clin Cancer Res. 2016年4月 15; 22(8): 1875-1884。
7Chmielewski M、Abken H. TRUCK:第四代CAR。Expert Opin Biol Ther. 2015;15(8):1145-54。
让我们开始对话
联系我们