Date: September 2017
在所有胰腺癌中,超过90%被归类为导管腺癌,在西方,胰腺癌是癌症相关死亡的第四大主要原因。胰腺癌的预后极差,患有III期不可切除肿瘤的患者的5年相对生存率为5%,中位生存期为3.5个月。1 不幸的是,胰腺癌的发病率一直在上升,而5年生存率却没有改变。手术切除是唯一可能治愈的疗法,但是只有10%的患者及早得到确诊可进行手术切除,而且大多数符合手术条件的患者最终会复发。和许多其他类型的癌症一样,胰腺癌可以悄无声息地生长多年,没有任何症状。大多数情况下,只有在癌症从胰腺外生长到其他近端组织和/或转移后才能得到确诊。这些患者几乎没有针对性的治疗方案。因此,迫切需要有效的新型疗法来治疗胰腺癌。
在过去15年里,被确诊为晚期胰腺癌的患者接受吉西他滨(Gemzar®)作为标准的一线治疗。临床前,我们使用吉西他滨作为标准疗法,为希望超越当前临床治疗选择或与新型疗法结合的客户提供基准;例如靶向药物和免疫调节剂。
临床前癌症研究界可以使用多种人类和鼠类胰腺细胞系,以帮助开发新型疗法。 Labcorp has a large panel of pancreatic lines ready for testing (see Table 1). 我们已经针对其中的几种模型优化并表征了皮下(SC)生长,并评估了它们对吉西他滨治疗的反应。
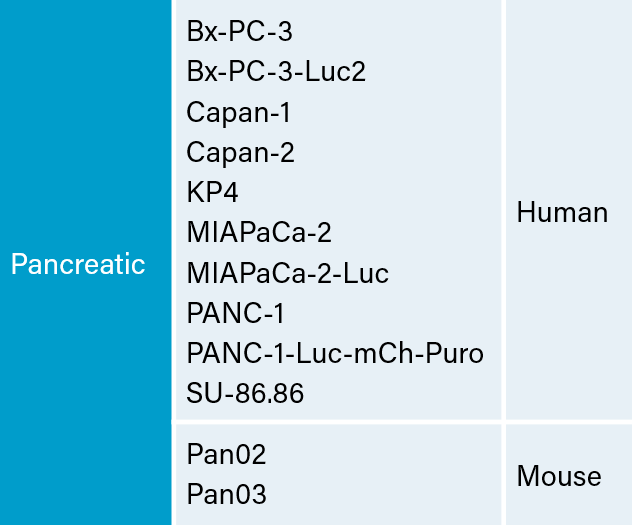
Pancreatic Carcinoma Cell Lines at Labcorp
PANC-1
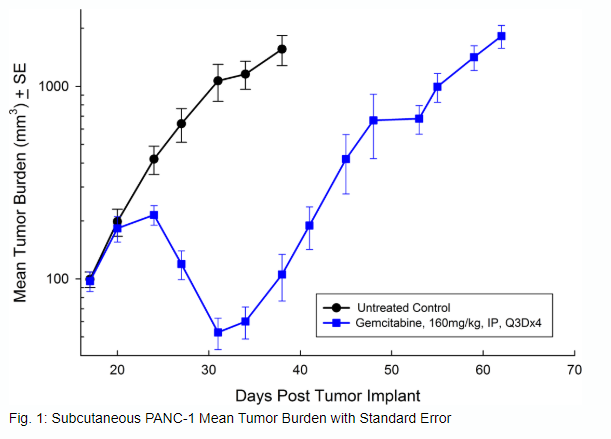
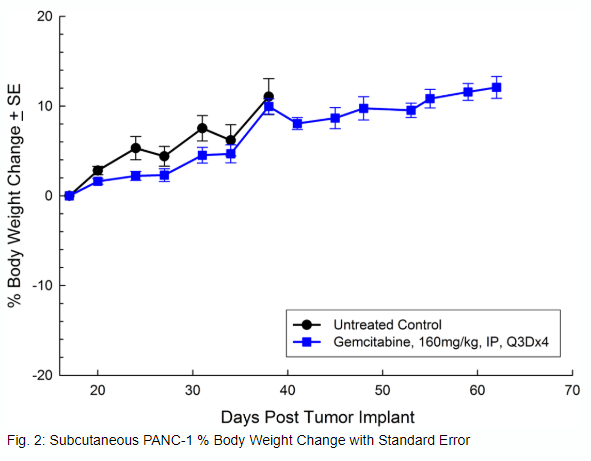
PANC-1分离自一名患有胰腺导管腺癌的56岁白人男性。皮下肿瘤生长可靠且一致,肿瘤体积每5天增加一倍,通常在植入后大约29天达到评估大小(~750mm3)。吉西他滨(160mg/kg)的治疗耐受性良好,并产生了统计学上显著的肿瘤生长延迟,但不能治愈(见图1和2)。
Capan-2
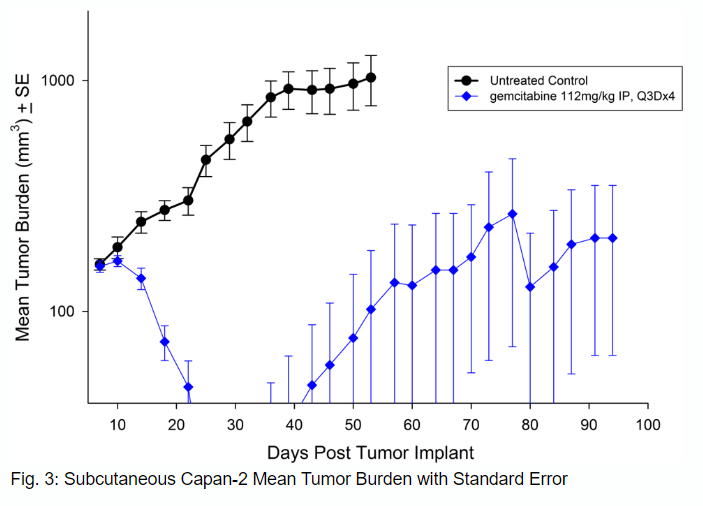
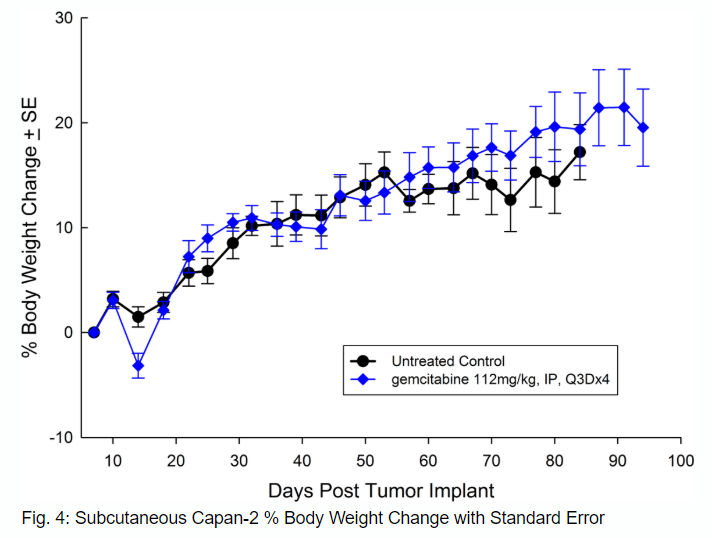
Capan-2分离自一名患有胰腺导管腺癌的56岁白人男性,其皮下肿瘤的生长比PANC-1要慢一些,肿瘤体积倍增时间约为12天,达到评估大小(750mm3)的时间为植入后约36天。吉西他滨(112mg/kg)的治疗耐受性良好,产生了统计学上显著的肿瘤生长延迟,并且有大量无肿瘤的幸存者(见图3和4)。
Bx-PC-3
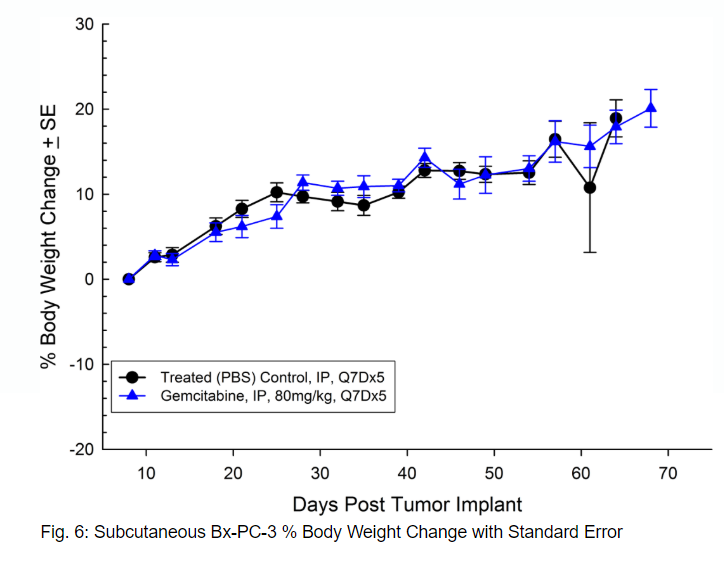
PANC-3分离自一名患有胰腺导管腺癌的61岁白人女性。皮下肿瘤生长导致肿瘤体积倍增时间约16天,达到评估大小(750mm3)的时间为植入后约38天。吉西他滨(80mg/kg)的治疗耐受性良好,但未能产生统计学上显著的肿瘤生长延迟(见图5和6)。
MIAPaCa-2
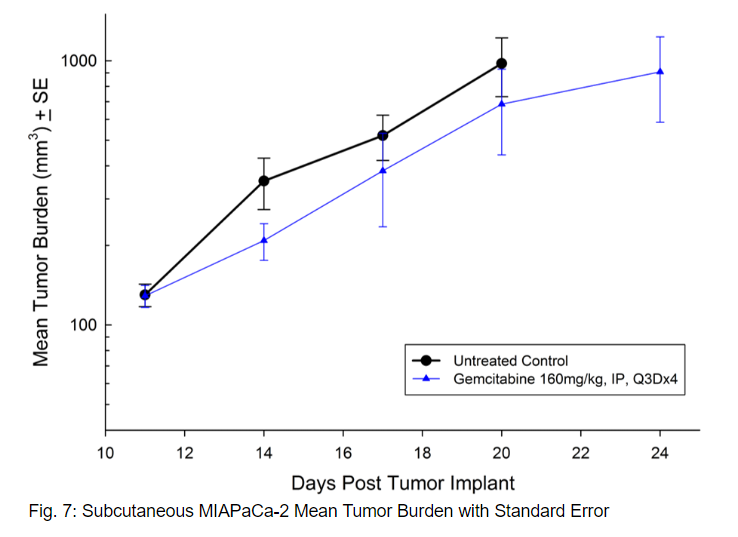
MIAPaCa-2分离自一名患有胰腺导管腺癌的65岁白人男性。该模型显示出极具侵袭性的皮下肿瘤生长,肿瘤体积倍增时间约为3天,达到评估大小(750mm3)的时间为植入后约21天。吉西他滨(160mg/kg)的治疗耐受性良好,产生了统计学上显著的肿瘤生长延迟,研究中观察到一名无肿瘤的幸存者(见图7和8)。
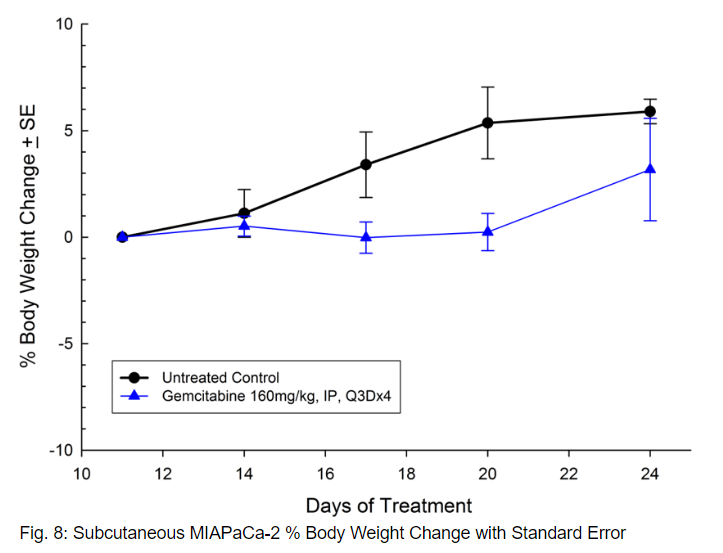
如同对治疗标准的临床反应一样,临床前的治疗反应高度依赖于所使用的肿瘤系。有许多因素可导致对吉西他滨治疗的反应性或缺乏反应性。但是,观察同一适应症的多种不同肿瘤系可以提供有关新疗法临床功效的关键信息。
让我们开始对话
联系我们