治疗性抗体或抗体样分子的组织交叉反应性评估是一项重要的临床前研究,此项研究是监管研究性新药(IND)或临床试验申请(CTA)的组成部分之一。
TCR为一系列体外免疫组织化学(IHC)筛查测定,主要用于识别非靶向结合,但同时也用于识别之前未知的潜在靶向结合位点。
冷冻的体外组织中是否存在IHC染色可用于提供潜在的体内器官毒性指征,以及为选择用于产生临床前安全性数据的动物毒性模型提供更多的依据。

治疗性抗体或抗体样分子的组织交叉反应性评估是一项重要的临床前研究,此项研究是监管研究性新药(IND)或临床试验申请(CTA)的组成部分之一。
TCR为一系列体外免疫组织化学(IHC)筛查测定,主要用于识别非靶向结合,但同时也用于识别之前未知的潜在靶向结合位点。
冷冻的体外组织中是否存在IHC染色可用于提供潜在的体内器官毒性指征,以及为选择用于产生临床前安全性数据的动物毒性模型提供更多的依据。
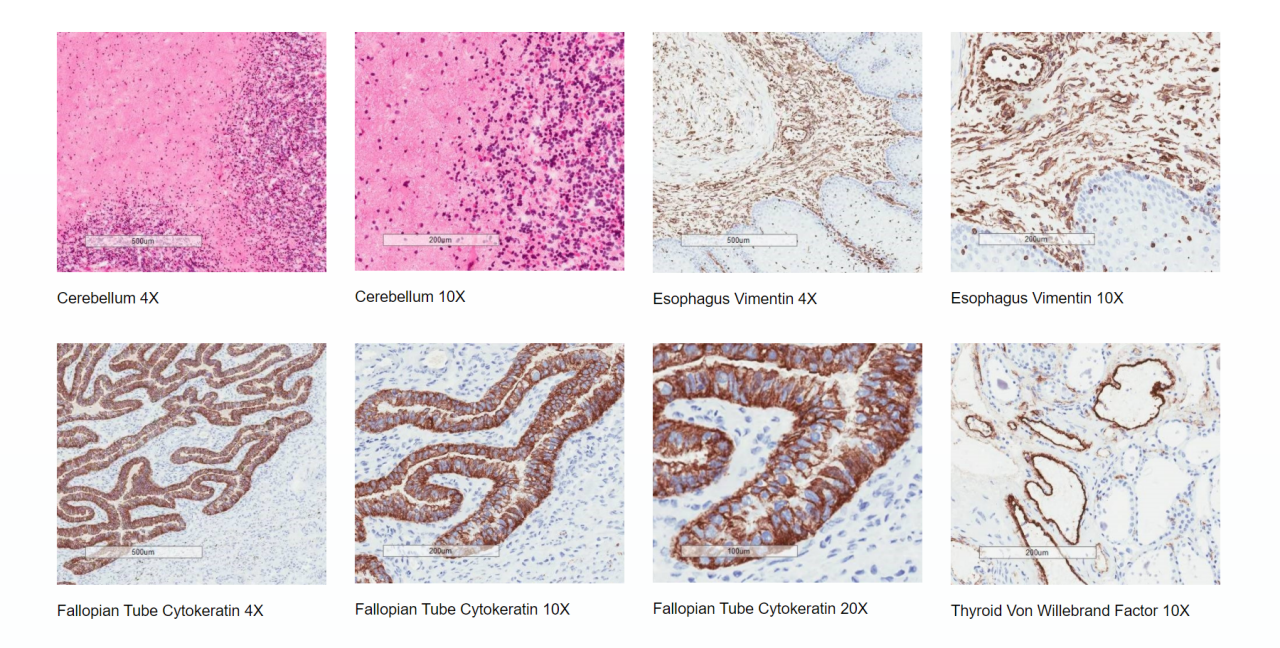
对于大多数生物治疗药物的IND/CTA申报,进行预期的TCR研究主要是为了识别非靶向结合,但同时也用于搜索之前未知的靶向结合位点。此类研究可用于提供潜在的体内器官毒性指征,同时对人类和动物组织的染色模式进行比较,从而为选择用于产生其他临床前安全性数据的动物毒性模型提供更多的依据。
TCR研究在徕博科位于英国哈罗盖特和亨廷顿的试验中心内进行。这两个试验中心都加入了英国GLP合规性监测计划,此计划由英国GLP监控机构(UK GLPMA)实施,该监控机构隶属于英国药品和保健品管理局(Medicines and Healthcare Products Regulatory Authority,简称MHRA)。
位于哈罗盖特和亨廷顿的两个试验中心均从1997年起进行该研究。拥有免疫组织化学(IHC)和组织学经验的专业科学家团队全面参与研究过程,确保实现IHC染色方案的优化,以生成和交付有意义的数据。
对于人类TCR研究,徕博科可遵照美国FDA和EMA的要求获取所有的冷冻组织。两个试验中心均持有英国人体组织管理局(United Kingdom Human Tissue Authority,简称UK HTA)颁发的许可证。对于动物物种TCR研究,徕博科拥有来自所有最常用的毒理学模型(灵长类、微型猪、犬类、啮齿类)的冷冻组织。
如有需要,科文斯可执行定制抗体标记程序(例如Biotin、FITC、Alexa488)。如果标记程序被认定不合适,也可以采用预复合程序。我们了解供试品的数量可能有限,虽然在理想情况下,标记程序要求至少30mg的份量,但在必要时我们可以接受远少于该数量的供试品。我们很乐意与您进一步讨论TCR研究的其他供试品要求。
完成一项TCR研究所需的时间取决于IHC方案的开发和优化阶段。开发和优化一个合适、稳健的IHC方案通常需要6周以内的时间。继成功开发和优化IHC染色方案之后,一般可在6周内提供TCR测试的数据/报告草案。
所有的TCR研究将由经验丰富的病理学家负责进行评审。从IHC染色方案开发/优化,到组织样本染色,病理学家可在所有的研究阶段过程中与您讨论测试结果。对染色强度、细胞位置、组织分布和染色频率进行常规记录,但我们将乐于与您探讨是否纳入更多的特殊病理学终点标准。
让我们开始对话
联系我们